Edward F. Coyle, Ph.D.
SPORTS SCIENCE EXCHANGE
MÉTABOLISME DES GRAISSES PENDANT L’EXERCICE
SSE n° 59, volume 8 (1995), numéro 6
Edward F. Coyle, Ph. D.
Professeur, Department of Kinesiology and Health Education
The University of Texas at Austin
Austin, Texas
Membre du Comité d'examen en médecine sportive du GSSI
POINTS PRINCIPAUX
1. Les personnes emmagasinent de grandes quantités de masse grasse sous forme de triglycérides dans les tissus adipeux de même que dans les fibres musculaires (triglycérides intramusculaires). Pendant l’exercice, ces réserves de gras sont mobilisées et oxydées à des vitesses relativement lentes par rapport aux glucides emmagasinés dans le glycogène musculaire.
2. À mesure que l’exercice passe de léger à modéré, soit de à 25 à 65 % du VO2 max, la vitesse de mobilisation des acides gras à partir des tissus adipeux et leur concentration dans le sang diminuent, tandis que la vitesse d’oxydation totale des lipides augmente en raison d’une utilisation relativement importante de triglycérides intramusculaires. Les triglycérides intramusculaires sont également à l’origine de l’augmentation caractéristique de l’oxydation des lipides consécutive aux programmes habituels d’entraînement d’endurance.
3. L'apport en glucides alimentaires influe grandement sur la mobilisation et l’oxydation des graisses pendant l’exercice; lorsque les réserves de glucides sont suffisantes après un apport alimentaire, ce sont ces réserves qui constituent la source privilégiée d'énergie pendant l’exercice. Ce phénomène est d'une importance particulière lors d’un exercice intense parce que seulement les glucides (et non les graisses) peuvent être mobilisés et oxydés suffisamment rapidement pour répondre aux besoins énergétiques nécessaires aux contractions musculaires intenses.
INTRODUCTION
Les deux principales sources d’énergie pendant l’exercice musculaire sont les lipides (triglycérides) et les glucides (glycogène et glucose) emmagasinés dans l’organisme. Au cours des 30 dernières années, le nombre considérable de recherches effectuées et l’expérience pratique accumulée montrent que les réserves de glycogène dans les muscles et le foie jouent un rôle important pour réduire la fatigue et améliorer la performance sportive. Par exemple, il est bien connu qu’un régime alimentaire surtout constitué de glucides est nécessaire pour maintenir des réserves élevées de glycogène lors des séances d’exercice intense et qu’un tel régime semble être le plus approprié pour améliorer la performance lors de l’entraînement (Simonsen et coll., 1991). Les réserves de glycogène sont indispensables pour les athlètes, surtout parce que, pendant l'exercice, ils ne peuvent transformer que lentement en énergie leurs réserves de masse grasse. C’est pourquoi, quand les taux de glycogène musculaire et de glucose sanguin sont faibles, il faut réduire l’intensité de l’exercice à un niveau qui permet à l’organisme de transformer suffisamment de graisses en énergie, malgré sa capacité limitée. Avec un entraînement d’endurance, les athlètes peuvent augmenter nettement la vitesse d’oxydation des graisses par l’organisme, ce qui leur permet de s’entraîner plus longtemps avant d’être épuisés en raison de la perte de glycogène. Bien entendu, l’entraînement améliore aussi la capacité des athlètes à s’entraîner avec plus d'intensité, mais ils doivent continuer à tirer la plus grande partie de leur énergie des glucides pendant une période d’entraînement ou de compétition intense, étant donné que leur plus grande capacité à oxyder les graisses ne peut répondre aux plus grandes demandes d’énergie.
Qu’est-ce qui ralentit la vitesse de transformation de la masse grasse en énergie pendant l’exercice ? De récentes recherches utilisant de nouvelles techniques ont commencé à faire la lumière sur cette question et à en tirer des conclusions qui sont rapportées dans le présent article. Même si nous ne comprenons pas encore très bien comment fonctionne le métabolisme des lipides pendant l’exercice, nous disposons toutefois de suffisamment de données pour jeter de sérieux doutes sur de nombreuses allégations publicitaires vantant les mérites de certains régimes alimentaires et de suppléments alimentaires contenant plus de lipides et moins de glucides.
RÉSERVES DE MASSE GRASSE
Tissus adipeux
Les graisses sont mises en réserve dans l’organisme sous forme de triglycérides, qui comprennent trois acides gras liés à une molécule de glycérol. Les acides gras se composent de chaînes d’atomes de carbone auxquels se rattachent des atomes d’hydrogène. Un gramme de lipides renferme plus d’énergie (9 kcal) qu’une masse équivalente de glucides (4 kcal/g). En général, il y a environ 50 000 à 60 000 kcal d’énergie emmagasinée sous forme de triglycérides dans toute la masse des adipocytes disséminés dans l'organisme. Une personne obèse aura évidemment emmagasiné plus d’énergie qu’une personne qui n’a que peu de masse grasse (Figure 1). Il faut dépenser environ 100 kcal d’énergie pour parcourir 1,6 km (1 mille) à pied, de sorte que la plupart d’entre nous ont suffisamment de réserves énergétiques de triglycérides pour marcher de 800 à 1 600 km (500 à 1 000 milles). Étant donné que cette grande quantité d’énergie est emmagasinée dans une masse relativement faible de triglycérides, ces derniers permettent aux personnes qui se déplacent de transporter leurs réserves d’énergie de la meilleure façon qui soit. En revanche, si toute cette énergie était stockée sous forme de glucides dans le glycogène, des molécules d’eau, qui sont très lourdes, se fixeraient aux molécules de glycogène, si bien que les réserves totales d’énergie pèseraient plus de 45 kg (100 lb). Le stockage d’énergie sous forme de triglycérides a très bien servi les populations nomades au cours de leur évolution quand la nourriture se faisait rare.
Triglycérides intramusculaires
Les triglycérides sont aussi directement emmagasinés sous forme de gouttelettes dans les fibres musculaires (triglycérides intramusculaires), amenant ainsi cette source d’énergie tout près du lieu d’oxydation dans les mitochondries des cellules musculaires. Les triglycérides intramusculaires représentent de 2 000 à 3 000 kcal d’énergie emmagasinée, ce qui en fait une plus grande source d’énergie potentielle que le glycogène musculaire, qui ne fournit qu’environ 1 500 kcal. Malheureusement, il s’avère difficile sur le plan technique de mesurer les triglycérides intramusculaires à partir de la biopsie d’un muscle, si bien que leur vitesse d’oxydation pendant l’exercice tout comme la façon dont ces réserves d’énergie varient en réaction à un entraînement intense ou à intervalles reste peu connue. Il est toutefois évident que, lors d'un exercice intense, les triglycérides intramusculaires ne peuvent fournir de l’énergie à moins d’un tiers de la vitesse attribuée au glycogène musculaire. Il faut donc savoir que l’énergie provenant des triglycérides intramusculaires pendant une période d’entraînement ou de compétition intense vient s’ajouter à celle fournie par le glycogène musculaire.
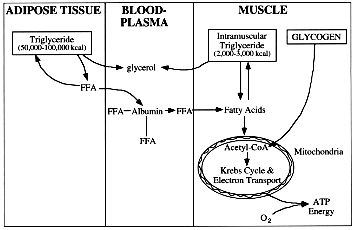
| Figure 1. Emmagasinage et mobilisation des réserves de triglycérides. Les triglycérides provenant des tissus adipeux peuvent se décomposer en glycérol et en acides gras libres (AGL), ces derniers étant mobilisés en se fixant sur l’albumine plasmatique pour être transportés par la circulation jusqu’aux muscles squelettiques et aux autres tissus. Les triglycérides intramusculaires peuvent aussi se décomposer en glycérol et en acides gras qui se rendent dans les mitochondries pour y être oxydés pendant l’exercice. |
Il faut également souligner que les triglycérides plasmatiques représentent une autre source d’énergie pour les muscles, en plus de l'énergie fournie par les triglycérides intramusculaires. Chez une personne à jeun, le foie produit une petite quantité de triglycérides liés à des lipoprotéines de très basse densité dans le sang. Même si les muscles peuvent décomposer ces triglycérides plasmatiques jusqu’à un certain point pendant l’exercice, leur apport énergétique demeure très faible (Kiens et coll., 1993).
MOBILISATION ET OXYDATION DES GRAISSES PENDANT L’EXERCICE
Mobilisation des acides gras libres à partir des tissus adipeux
Les importantes réserves de triglycérides dans les tissus adipeux sont mobilisées de façon relativement lente pendant un exercice. Au cours de ce processus, l’exercice stimule une enzyme, la lipase hormonosensible, afin de dissoudre les lipides ou les molécules de triglycérides en trois molécules d’acides gras libres (AGL) non liés et une molécule de glycérol (Figure 1); ce processus de décomposition des triglycérides s’appelle la lipolyse. Le glycérol libéré lors de cette réaction est soluble dans l’eau et se diffuse librement dans le sang. Sa vitesse de formation dans le sang fournit la mesure directe de la quantité de triglycérides hydrolysés dans l’organisme. L’augmentation d’adrénaline dans le sang, qui active les récepteurs bêta des adipocytes, serait le principal facteur responsable de la stimulation de la lipolyse des tissus adipeux pendant un exercice (Arner et coll., 1990); d’autres facteurs hormonaux jouent sans doute aussi un rôle.
Le sort des trois molécules d’acides gras libres libérées à partir des tissus adipeux lors de la lipolyse est complexe (Figure 1). Étant donné que ces acides gras ne sont pas hydrosolubles, ils doivent se fixer à un support protéique afin d’être transportés des cellules jusqu’à la circulation sanguine. Au repos, environ 70 % des acides gras libres libérés lors de la lipolyse se fixent donc aux molécules de glycérol afin de reformer des triglycérides au sein des adipocytes. Toutefois, lors d’un exercice de faible intensité, ce processus est atténué à mesure que la vitesse globale de lipolyse augmente; de ce fait, la vitesse de formation des acides gras libres dans le sang peut devenir jusqu’à cinq fois plus élevée (Klein et coll., 1994; Romijn et coll., 1993; Wolfe et coll., 1990). Une fois parvenue dans le sang, les molécules d’acides gras libres se fixent légèrement à l’albumine, une protéine plasmatique, avant d'être transportées dans la circulation. Une partie des acides gras se libèrent de l’albumine et se fixent aux protéines intramusculaires, qui, à leur tour, les transportent jusqu’aux mitochondries pour y être oxydés (Turcotte et coll., 1991).

| Figure 2. Contribution des quatre principaux substrats d’énergie à la dépense énergétique après 30 minutes d’exercice à 25 %, 65 % et 85 % de la consommation maximale d’oxygène chez les sujets à jeun. Reproduits avec l’autorisation de Romijn et coll. (1993). |
Des études récentes menées auprès d'hommes à jeun entraînés à l'endurance révèlent que la vitesse de formation des acides gras libres dans le sang diminue à mesure qu’augmente l’intensité de l’exercice, de faible (25 % du VO2 max, comparable à celle de la marche) à modéré (65 % du VO2 max, comparable à la plus grande foulée lors d'une course de 2 à 4 heures) et à élevé (85 % du VO2 max, le rythme le plus élevé qui peut être soutenu pendant 30 à 60 minutes) (Figure 2). L’apport des glucides (glycogène musculaire et glucose sanguin) et des lipides (AGL plasmatiques provenant des tissus adipeux en plus des triglycérides intramusculaires) à la dépense énergétique totale pendant l’exercice à diverses intensités est présenté dans la Figure 2. Il faut souligner que l’oxydation totale des graisses augmente même si de moins en moins d’AGL plasmatiques contribuent aux besoins énergétiques à mesure que l’intensité de l’exercice augmente de 25 % à 65 % du VO2 max. De plus, même si l’organisme diminue proportionnellement le recours aux AGL plasmatiques dans la production d’énergie au fur et à mesure que l’exercice s’intensifie de 25 % à 65 % du VO2 max, ne saurait être écartée la possibilité qu’à une intensité intermédiaire, p. ex., à 45 % du VO2 max, les AGL plasmatiques puissent fournir plus d’énergie qu’à 25 % du VO2 max.
Oxydation des triglycérides intramusculaires pendant l’exercice
Depuis un certain temps déjà, il est reconnu que les triglycérides intramusculaires jouent sûrement un rôle important dans l’oxydation des graisses pendant l’exercice à certaines intensités (Essen et coll., 1977), et particulièrement chez les chiens (Issekutz et Paul , 1968). Au cours d’un exercice de faible intensité, comme à 25 % du VO2 max, les AGL plasmatiques représenteraient presque l’unique source d’énergie provenant des lipides étant donné que la vitesse d’oxydation des graisses correspond de très près à la vitesse où les molécules d’AGL disparaissent du sang. Toutefois, lors d’un exercice très intense, l’oxydation totale des graisses chez les personnes entraînées à l'endurance surpasse de beaucoup la vitesse de disparition des AGL plasmatiques, indiquant qu’il se produit une oxydation supplémentaire des graisses à partir d’un réservoir de triglycérides intramusculaires. Ce résultat est illustré dans les figures 2 et 3. À l'aide de calculs, il a été observé que les triglycérides intramusculaires sont très peu oxydés pendant un exercice à 25 % du VO2 max, tandis qu’à 65 % du VO2 max, ils représentent environ la moitié de l’oxydation totale des graisses. D'après les mêmes calculs, l’oxydation des triglycérides intramusculaires diminue quelque peu pendant un exercice à 85 % du VO2 max. Ces observations étant au stade préliminaire, il faut effectuer d’autres recherches pour élucider pleinement l’effet de l’intensité de l’exercice, du régime alimentaire et de l’entraînement sur l’oxydation des triglycérides intramusculaires.
Oxydation globale de la masse grasse pendant un exercice à intensité croissante
L’effet de l’intensité de l’exercice sur l’oxydation des graisses et la provenance de ces graisses suscitent un vif intérêt. Selon plusieurs, l’exercice doit être de faible intensité pour permettre une combustion optimale des graisses. Toutefois, selon les figures 2 et 3, la vitesse de l’oxydation totale des graisses est plus élevée à 65 % qu’à 25 % du VO2 max, et s'élève à 110 cal · kg-1 · min-1 par rapport à 70 cal · kg-1 · min-1. À 25 % du VO2 max, la presque totalité de la dépense énergétique pendant l’exercice provient des lipides, tandis qu’elle ne provient qu’à moitié de l’oxydation des graisses à 65 % du VO2 max. Toutefois, étant donné que le taux de dépense totale d’énergie est si élevé (2,6 fois plus) à 65 % du VO2 max, la valeur absolue de la vitesse d’oxydation des graisses est également plus élevée, c.-à-d. qu’elle représente la moitié d’une valeur beaucoup plus élevée (Figure 3). Il peut donc s’avérer trompeur d’exprimer l’énergie obtenue des lipides comme un simple pourcentage de la dépense énergétique sans tenir compte du taux de dépense totale d’énergie. Pareillement, la baisse dans la vitesse de formation des AGL plasmatiques à mesure que l’exercice s’intensifie ne prouve pas qu’un exercice de faible intensité constitue le meilleur moyen de diminuer les réserves de graisse des tissus adipeux.

| Figure 3. Vue agrandie des sources de lipides oxydés pendant un exercice à 25 % (pas de marche), 65 % (course modérée) et 85 % (course intense) de la consommation maximale d’oxygène chez des sujets à jeun. |
Tant le taux de dépense énergétique que la durée de l’exercice sont essentiels pour déterminer la perte de masse grasse. Il faut également tenir compte de l’effet de l’exercice sur la dépense énergétique lors des périodes de récupération entre chaque séance d’exercice. La diminution des réserves de masse grasse après un entraînement physique prolongé dépend surtout de la dépense totale d’énergie par jour et pas seulement de la source d’énergie effectivement oxydée pendant l’exercice (Ballor et coll., 1990).
SUPPLÉMENTS ALIMENTAIRES DE LIPIDES PENDANT L’EXERCICE
Consommation de triglycérides à longue chaîne
Il n'est pas possible de consommer des acides gras libres en raison de leur trop grande acidité et du besoin d’un support protéique pour permettre leur absorption par l'intestin. La consommation de triglycérides représente donc le seul moyen pratique d’augmenter de façon importante la concentration de lipides dans le sang. Les triglycérides à longue chaîne normaux intègrent la circulation sanguine de 3 à 4 heures après leur ingestion et sont liés aux chylomicrons, des transporteurs des lipoprotéines dans le sang. La vitesse de dégradation des triglycérides liés aux chylomicrons du sang et la vitesse de leur absorption par les muscles pendant l’exercice sont relativement faibles et ces triglycérides servent principalement à reconstituer les réserves de triglycérides intramusculaires pendant la récupération après l’exercice (Mackie et coll., 1980; Oscai et coll., 1990). Par conséquent, même si ce n'est pas encore prouvé, il est peu probable que la consommation de triglycérides à longue chaîne offre de grandes possibilités en tant que source d’énergie importante pour les muscles pendant l’exercice (Terjung et coll., 1983) .
Consommation de triglycérides à chaîne moyenne
Contrairement aux triglycérides à longue chaîne, les triglycérides à chaîne moyenne (TCM) sont absorbés directement dans le sang et le foie après leur ingestion où ils sont rapidement décomposés en acides gras et en glycérol. En théorie, ils offrent donc la possibilité d’augmenter rapidement la concentration d’AGL plasmatiques. Les triglycérides à chaîne moyenne présentent un autre avantage théorique étant donné qu’ils semblent être facilement transportés dans les cellules jusqu’aux mitochondries pour y être oxydés. Des études récentes montrent qu’une forte proportion des triglycérides à chaîne moyenne subissent une oxydation, qui augmente plus rapidement lorsque des lipides sont consommés en même temps que des glucides (Jeukendrup et coll., 1995). Toutefois, la plupart des gens ne peuvent consommer plus de 30 g de triglycérides à chaîne moyenne sans éprouver de graves malaises gastro-intestinaux et de la diarrhée. C’est pourquoi l’ingestion de triglycérides à chaîne moyenne ne fournit que 3 à 6 % de la dépense énergétique totale pendant l’exercice (Jeukendrup et coll., 1995). De plus, si la consommation de triglycérides à chaîne moyenne s’accompagne de glucides, la sécrétion d’insuline induite par les glucides inhibe partiellement la mobilisation des réserves de masse grasse dans l’organisme, entraînant ainsi une grande réduction de l’oxydation des graisses comparativement l'exercice effectué à jeun.
Perfusions intraveineuses de lipides pour augmenter concentration des AGL plasmatiques
En recherche, une technique utilisée pour augmenter la concentration des AGL plasmatiques consiste à administrer une perfusion intraveineuse d’une émulsion de triglycérides, comme l’Intralipid®, suivie d’une perfusion d’héparine, ce qui libère dans le sang une enzyme lipolytique, la lipoprotéine lipase, à partir de ses réserves dans les tissus adipeux et les muscles, et entraîne le fractionnement des triglycérides en glycérol et en acides gras libres par l’enzyme (Vukovich et coll., 1993). Il faut surveiller attentivement les vitesses de perfusion étant donné qu’une trop grande augmentation d’acides gras libres dans le sang est nocive. Dans certains cas, la concentration des AGL plasmatiques devient inférieure à la valeur optimale pendant l’exercice, si bien qu’il pourrait être avantageux, en théorie, de l’augmenter artificiellement. Ainsi, la mobilisation et la concentration des AGL plasmatiques sont faibles lors d’un exercice intense (évoqué précédemment) de même que lors d’un exercice après consommation de glucides, comme nous le verrons ci-dessous. Dans ces conditions, la vitesse d’oxydation du glycogène musculaire peut être légèrement réduite en augmentant la concentration des acides gras libres par perfusion intraveineuse de triglycérides et d’héparine (Costill et coll., 1977; Vukovich et coll., 1993). Toutefois, comme il s’agit d’un effet relativement faible, il reste à démontrer si cette façon de procéder peut avoir des effets positifs sur la performance.
L’ENTRAÎNEMENT D’ENDURANCE AUGMENTE L’OXYDATION DES GRAISSES PENDANT L’EXERCICE, MAIS NON LA MOBILISATION DES ACIDES GRAS LIBRES DANS LE SANG
Source d'une augmentation de l’oxydation des graisses
Comme indiqué dans une édition récente de Sports Science Exchange (Terjung, 1995), l’une des adaptations les plus fonctionnelles de l’entraînement d’endurance consiste à faire augmenter la taille et le nombre des mitochondries musculaires, améliorant ainsi grandement le métabolisme aérobie ou la capacité des muscles à utiliser l’oxygène pour métaboliser les graisses et les glucides afin de produire de l’énergie. Lors d’un exercice d'une intensité sous-maximale absolue, les personnes entraînées à l'endurance ressentent moins de fatigue musculaire, leur bilan énergétique est moins déséquilibré et elles dépendent moins du glycogène musculaire comme source d’énergie que les personnes non entraînées. Une diminution de l’utilisation du glycogène s’accompagne d’une augmentation de l’oxydation des graisses et deux études ont été effectuées pour trouver la source de cette dégradation supplémentaire de lipides.
| Figure 4. Substrats fournissant l’énergie pendant l’exercice à une intensité absolue (64 % du VO2 max d’avant l’entraînement). Mesures prises quand les sujets n’étaient pas entraînés (avant l’entraînement) et étaient entraînés (après l’entraînement) à l’endurance pendant 12 semaines. Après l’entraînement, l’oxydation des glucides et des AGL plasmatiques diminue, tandis que l’utilisation des triglycérides intramusculaires augmente. Les différences statistiquement significatives entre les valeurs avant et après entraînement sont indiquées par un *. Redessinée à partir de Martin et coll. (1993) avec leur autorisation. |
Ces deux études ont donc mesuré l’apport des triglycérides intramusculaires et des AGL plasmatiques lors d’un exercice à 64 % du VO2 max obtenu avant l’entraînement, avant et après 12 semaines de séances de course et de cyclisme éreintantes (Hurley et coll., 1986; Martin et coll., 1993). La Figure 4 résume les résultats de ces études. La réduction de l’oxydation du glycogène musculaire après un entraînement d’endurance est directement associée à une augmentation de l’oxydation des triglycérides provenant de l’intérieur des muscles et non du sang. Les facteurs expliquant la plus grande utilisation des triglycérides intramusculaires sont mal connus. En principe, la hausse de concentration des triglycérides intramusculaires déjà observée après l’entraînement (Morgan et coll., 1969) pourrait avoir joué un rôle, mais une telle hausse ne semble pas s’être produite dans les deux études dont il est question. Curieusement, la vitesse de disparition des AGL plasmatiques a effectivement diminué après l’entraînement. Cette observation indique que, si l'exercice est d'une intensité modérée, la mobilisation et l’oxydation des acides gras ne changent pas beaucoup après un entraînement d’endurance. Comme nous le verrons ci-dessous, ce résultat concorde avec ceux des études transversales comparant les personnes non entraînées avec des personnes entraînées à l'endurance lors d'un exercice de faible intensité. Il semble donc que les triglycérides intramusculaires soient la principale source de lipides, qui s’oxydent plus rapidement en s'adaptant à l’entraînement d’endurance, et que l’oxydation de ce gras intramusculaire est associée à une baisse de l’utilisation du glycogène musculaire et à une amélioration de l’endurance physique.
Nous avons récemment comparé la vitesse de mobilisation des AGL plasmatiques et la lipolyse de l'organisme entier chez des hommes non entraînés à celles d'hommes entraînés à l'endurance (Klein et coll., 1994). Au cours de cet essai, les deux groupes ont marché sur un tapis roulant pendant 4 heures à une cadence rapide qui exigeait un VO2 de 20 · kg-1 · min-1. Cet effort exigeait environ 28 % du VO2 max chez les sujets entraînés comparativement à 43 % du VO2 max chez les sujets non entraînés. Tel que prévu, l’oxydation globale de masse grasse chez les sujets entraînés était d’environ un tiers plus élevée que chez les sujets non entraînés. Il est intéressant de noter que, lors d'un exercice dont l'intensité était peu élevée, nous nous attendions à une faible utilisation des triglycérides intramusculaires; nous avons dû constater que la rapidité de disparition des AGL plasmatiques correspondait de façon très rapprochée à la vitesse totale d’oxydation des lipides chez les sujets entraînés. Ce résultat indique que les personnes entraînées à l'endurance sont capables d’oxyder les acides gras provenant des tissus adipeux au même rythme auquel ils sont mobilisés. Chez les sujets non entraînés, en revanche, même si leurs vitesses de lipolyse globale et de mobilisation des AGL plasmatiques étaient identiques à celles des sujets entraînés, leur vitesse d’oxydation des graisses était plus faible. Les sujets entraînés semblaient pouvoir oxyder une plus grande partie des AGL provenant de la circulation même si la vitesse de disparition des AGL plasmatiques était semblable dans les deux groupes. Ce phénomène montre que les sujets non entraînés sont davantage en mesure de mobiliser les AGL que de les oxyder, si bien qu’une partie importante des AGL mobilisés sont réintégrés dans les triglycérides de certains tissus. La principale adaptation à l’exercice des sujets entraînés leur permettant d’oxyder plus de lipides lors de la marche semble provenir d’une plus grande capacité des muscles d’oxyder les AGL plutôt que d’une plus grande mobilisation des AGL à partir des tissus adipeux dans le sang.
EFFET DES GLUCIDES ALIMENTAIRES SUR L’OXYDATION DES GRAISSES PENDANT L’EXERCICE
Consommation de glucides alimentaires dans les heures qui précèdent l’exercice
L’oxydation des graisses pendant l’exercice est très sensible à la durée de l’intervalle entre la consommation de glucides et le début de l’exercice ainsi qu’à la durée de l’exercice. Cet effet est dû en partie à l’augmentation du taux plasmatique d’insuline après un repas de glucides et de l’inhibition de la lipolyse dans les tissus adipeux qui s’ensuit, réduisant ainsi la concentration des AGL dans le sang. Cet l’effet dure au moins 4 heures après avoir consommé 140 g de glucides à indice glycémique élevé (Montain et coll., 1991). Dans ces conditions, un apport en glucides réduit à la fois l’oxydation totale des graisses et la concentration des AGL plasmatiques pendant les premières 50 minutes d’exercice d'une intensité modérée. Toutefois, cette suppression de l’oxydation des graisses s’inverse à mesure que l’exercice se prolonge; après 100 minutes d’exercice, la vitesse d’oxydation des graisses devient la même, peu importe qu'il y ait eu consommation ou non de glucides avant l’exercice. Il semble que l’organisme dépende fortement des glucides, mais moins des lipides, après la consommation de glucides dans les quelques heures qui précèdent; ce qui revient à dire que, quand les glucides sont en quantité suffisante, ils constituent la source d'énergie privilégiée. L’insuline joue sans doute un rôle pour réguler la part de glucides et de lipides oxydés pendant l’exercice.
La réduction de l’oxydation des graisses et la plus grande oxydation des glucides ne nuit généralement pas à condition que cette dernière provienne entièrement du glucose sanguin acquis par la consommation de glucides, évitant ainsi l’utilisation du glycogène musculaire. À l’heure actuelle, peu d’éléments permettent de recommander de s'abstenir de consommer des glucides avant l’exercice, étant donné qu'un tel apport ne fera que déplacer le métabolisme énergétique qui dépend alors davantage de l’oxydation des AGL plasmatiques et moins de l’oxydation du glucose sanguin, tout en diminuant les effets sur le glycogène musculaire et l’utilisation des triglycérides intramusculaires.
La mobilisation des AGL plasmatiques est étonnamment sensible aux moindres augmentations de taux d’insuline dans le sang (Jensen et coll., 1989), et il semble que la lipolyse soit affectée pendant une longue période après un apport en glucides (Montain et coll., 1991). Les régimes faibles en glucides, ou contenant des glucides qui entraînent moins de sécrétion d’insuline, activent certainement encore suffisamment la réaction insulinique pour réduire la mobilisation des AGL plasmatiques. Par conséquent, tout produit ou régime qui prétend augmenter la mobilisation et l’oxydation des AGL plasmatiques devrait pouvoir éliminer la presque totalité de la réaction insulinique aux glucides présents dans leur produit, ce qui semble très improbable. À tout le moins, les fabricants de ces produits doivent-ils prouver que leur régime augmente la mobilisation des AGL et procure certains avantages. Tel qu'indiqué plus haut, une plus grande mobilisation des AGL ne serait certainement d’aucune valeur pour les personnes non entraînées, puisque leur capacité à mobiliser les AGL est supérieure à celle qu'ont leurs muscles de les oxyder.
Élimination des glucides alimentaires chez les personnes entraînées à l'endurance
Sachant que même de faibles quantités de glucides alimentaires peuvent affecter le métabolisme lipidique, Phinney et coll. (1983) ont effectué une étude au cours de laquelle des hommes entraînés à l'endurance ont consommé des aliments riches en lipides et ne contenant presque pas de glucides, soit moins de 20 g/j pendant 4 semaines. Un tel régime a permis de diminuer le taux de glycogène musculaire de moitié, et l’oxydation des graisses a augmenté de façon remarquable lors d’un exercice d'intensité modérée, allant de 62 à 64 % du VO2 max. Toutefois, ce régime n’a pas augmenté la durée de l'effort soutenu, en dépit d’une augmentation de l’oxydation des graisses. De plus, les sujets n'ont pas été en mesure de faire des exercices d'une intensité plus élevée. Il semble évident que même un régime aussi extrême ne peut permettre une augmentation suffisante de l'oxydation des graisses pour remplacer tout le glycogène musculaire comme source d’énergie dans le cas d'un exercice intense. De plus, un apport alimentaire élevé en lipides constitue un facteur de risque de cardiopathies et autres maladies.
RÉSUMÉ
Les personnes emmagasinent de grandes quantités de masse grasse sous forme de triglycérides dans les tissus adipeux de même que dans les fibres musculaires. Pendant l’exercice, ces réserves de gras sont mobilisées et oxydées à des vitesses relativement lentes par rapport aux glucides emmagasinés dans le glycogène musculaire. Les acides gras provenant des tissus adipeux sont mobilisés dans le sang et transportés par l’albumine jusqu’aux muscles pour y être oxydés. La mobilisation des acides gras libres dans le sang diminue à mesure qu’augmente l’intensité de l’exercice, de faible (25 % du VO2 max) à modéré (65 % du VO2 max) et à élevé (85 % du VO2 max). Toutefois, l’oxydation totale des graisses augmente à mesure que l’intensité de l’exercice augmente de 25 % à 65 % du VO2 max en raison de l’oxydation des triglycérides intramusculaires, qui représentent environ la moitié des lipides oxydés. L’entraînement d’endurance augmente de façon caractéristique l’oxydation des graisses lors d’un exercice d'intensité modérée en accélérant l’oxydation des triglycérides intramusculaires sans augmenter la mobilisation ni l’oxydation des acides gras libres dans le sang. De même, au cours d’un exercice de faible intensité avec très peu d’oxydation des triglycérides intramusculaires, l’oxydation plus importante des graisses chez les personnes entraînées ne semble pas due à la plus grande mobilisation des acides gras libres dans le sang, mais à leur plus grande vitesse d’oxydation une fois que les AGL sont disparus du sang en raison de l’exercice. Il semble donc que les personnes non entraînées ont une plus grande capacité à mobiliser plutôt qu’à oxyder les acides gras libres lorsqu’elles font de l’exercice à jeun. La consommation de glucides dans les heures qui précèdent l’exercice, même en quantités relativement faibles, réduit l’oxydation des graisses lors d’un exercice, surtout par l’action de l’insuline. Les suppléments alimentaires de lipides ou un régime alimentaire spécial ne sont guère en mesure d’augmenter l’oxydation des graisses, surtout lors de compétitions sportives. Les réserves de masse adipeuse ou les suppléments alimentaires de lipides ne peuvent donc remplacer adéquatement le glycogène musculaire et le glucose sanguin comme sources d’énergie lors d’un exercice intense.
References
Arner, P., E. Kriegholm, P. Engfeldt, and J. Bolinder (1990). Adrenergic regulation of lipolysis in situ at rest and during exercise. J. Clin. Invest. 85:893-898.
Ballor, D.L., J.P. McCarthy and E.J. Wilterdink (1990). Exercise intensity does not affect the composition of dietand exercise-induced body mass loss. Am J Clin Nutr. 51:142-146.
Costill, D.F., E.F. Coyle, G. Dalsky, W. Evans, W. Fink, and D. Hoopes. (1977). Effects of elevated plasma FFA and insulin on muscle glycogen usage during exercise. J. Appl. Physiol. 43: 695-699.
Coyle, E.F., A.R. Coggan, M.K. Hemmert, R.C. Lowe, and T.J. Walters (1985). Substrate usage during prolonged exercise following a preexercise meal. J. Appl. Physiol. 59:429-433.
Essen, B., L. Hagenfeldt, and L. Kaijser (1977). Utilization of blood-borne and intramuscular substrates during continuous and intermittent exercise in man. J. Physiol. 265:489-506.
Hurley, B.F., P.M. Nemeth, W.H. Martin, J.M. Hagberg, G.P. Dalsky, and J.O. Holloszy (1986). Muscle triglyceride utilization during exercise: effect of training. J. Appl. Physiol. 60:562-567. Issekutz, B., and B. Paul (1968). Intramuscular energy sources in exercising normal and pancreatectomized dogs. Am. J. Physiol. 215(1):197-204.
Jensen, M.D., M. Caruso, V. Heiling, and J.M Miles (1989). Insulin regulation of lypolysis in nondiabetic and IDDM subjects. Diabetes 38:1595-1601.
Jeukendrup, A.E., W.H.M. Saris, P. Schrauwen, F. Brouns, and A.J.M. Wagenmakers (1995). Metabolic availability of medium-chaim triglycerides coingested with carbohydrate during prolonged exercise. J. Appl. Physiol. 79: 756-762.
Kiens, B., B. Essen-Gustavsson, N.J. Christensen, and B. Saltin (1993). Skeletal muscle substrate utilization during submaximal exercise in man: effect of endurance training. J. Physiol. (London) 469: 459-478.
Klein, S., E.F. Coyle, and R.R. Wolfe (1994). Fat metabolism during low-intensity exercise in endurance-trained and untrained men. Am. J. Physiol. 267 (Endocrinol. Metab. 30):E934-E940. Mackie, B.G., G.A. Dudley, H. Kaciuba-Uscilko, and R.L. Terjung (1980). Uptake of chylomicron triglycerides by contracting skeletal muscle in rats. J. Appl. Physiol. 49: 851-855.
Martin, W.H., G.P. Dalsky, B.F. Hurley, D.E. Matthews, D.M. Bier, J.O. Hagberg, and J.O. Holloszy (1993). Effect of endurance training on plasma FFA turnover and oxidation during exer-
cise. Am. J. Physiol. 265 (Endocrinol. Metab. 28):E708-E714.
Montain, S.J., M.K. Hopper, A.R. Coggan, and E.F. Coyle (1991). Exercise metabolism at different time intervals after a meal. J. Appl. Physiol. 70(2):882-888.
Morgan, T.E., F.A. Short, and L.A. Cobb (1969). Effect of long-term exercise on skeletal muscle lipid composition. Am. J. Physiol. 216:82-86.
Oscai, L.B., D.A. Essig, and W.K. Palmer (1990). Lipase regulation of muscle triglyceride hydrolysis. J. Appl. Physiol. 69: 1571-1577.
Phinney, S.D., Bistrian, W.J. Evans, E. Gervino, and G.L. Blackburn (1983). The human metabolic response to chronic ketosis without caloric restriction: preservation of submaximal exercise capability with reduced carbohydrate oxidation. Metabolism 32:769-776.
Romijn, J.A., E.F. Coyle, L.S. Sidossis, A. Gastaldelli, J.F. Horowitz, E. Endert, and R.R. Wolfe (1993). Regulation of endogenous fat and carbohydrate metabolism in relation to exercise
intensity and duration. Am. J. Physiol. 265 (Endocrinol. Metab. 28):E380-E391.
Simonsen, J.C., W.M. Sherman, D.R. Lamb, A.R. Dernbach, J.A. Doyle, and R. Strauss (1991). Dietary carbohydrate, muscle glycogen, and power during rowing training. J. Appl. Physiol. 70: 1500-1505.
Terjung, R. (1995). Muscle adaptations to aerobic training. Sports Sci. Exchange 8(54), Number 1.
Terjung,R.L. B. G. Mackie, G.A. Dudley, and H. Kaciuba-Uscilko (1983). Influence of exercise on chylomicron triacylglycerol metabolism: plasma turnover and muscle uptake. Med. Sci.
Sports Exerc. 15: 340-347.
Turcotte, L.P., B. Kiens and E.A. Richter (1991). Saturation kinetics of palmitate uptake in perfused skeletal muscle. FEBS Letters 279: 327-329.
Vukovich, M.D., D.L. Costill, M.S. Hickey, S.W. Trappe, K.J. Cole, and W.J. Fink (1993). Effect of fat emulsion infusion and fat feeding on muscle glycogen utilization during cycle exercise. J. Appl. Physiol. 75: 1513-1518.
Wolfe, R.R., S. Klein, F. Carraro, and J.-M. Weber (1990). Role of triglyceride-fatty acid cycle in controlling fat metbolism in humans during and after exercise. Am. J. Physiol. 258
(Endocrinol. Metab. 21):E382-E389.